Američka agencija za lekove FDA zvanično je pre tri dana odobrila za primenu ćelijiski proizvod Omisirge proizvođača Gamida, ranije poznat kao „Omidubicel”. Ovim je prvi put u istoriji zvanično odobren za korišćenje proizvod nastao umnožavanjem i kultivisanjem krvi pupčanika.
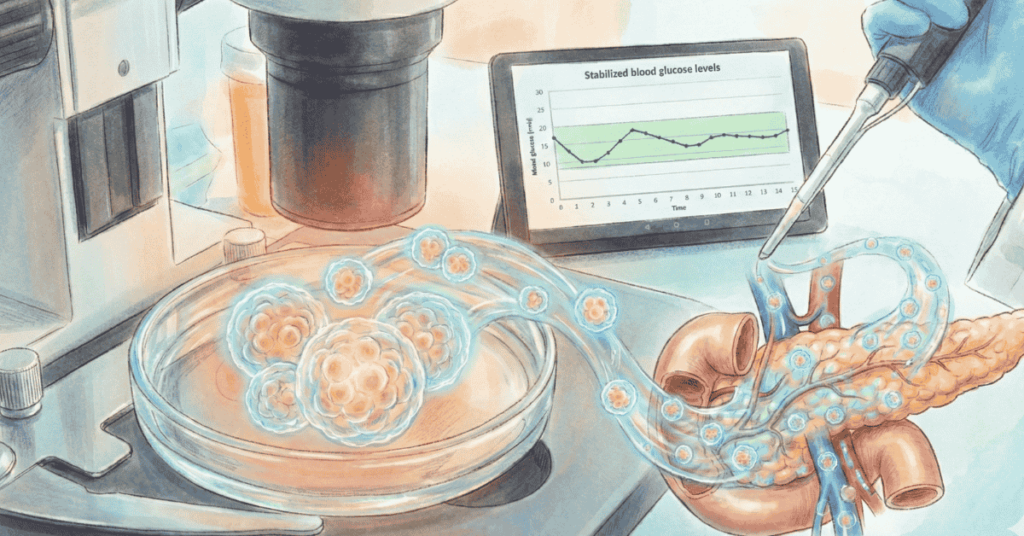
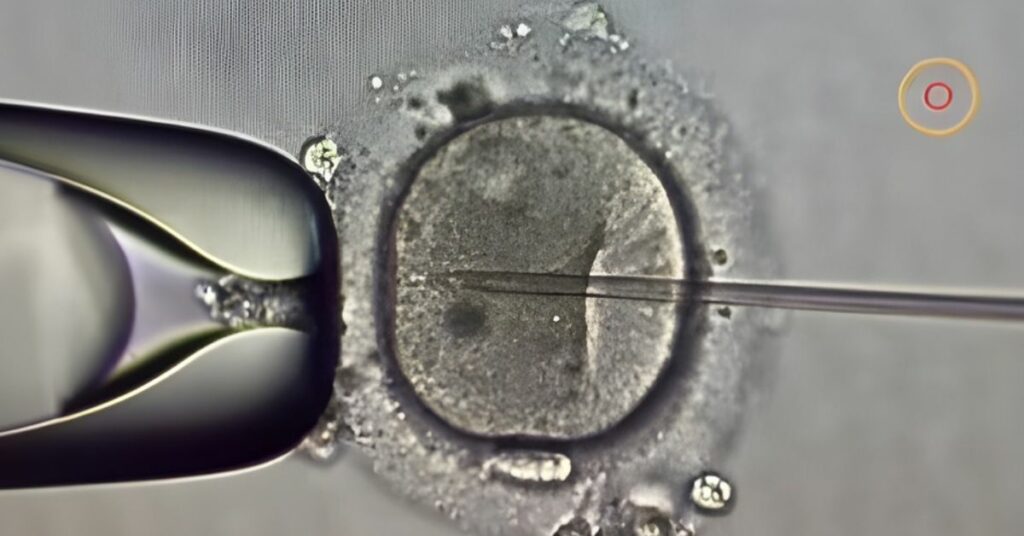
Krv pupčanika je kultivisana u strogo kontrolisanim laboratorijskim uslovima kako bi se selektivno povećao broj matičnih ćelija i dobile osobine koje su do sada predstavljale ograničavajući faktor za širu primenu ovog izvora matičnih ćelija.
Omisirge je namenjen pre svega pacijentima koji nisu pronašli odgovarajućeg donora matičnih ćelija za transplantaciju.
.jpg) Foto: Freepik
Foto: Freepik
Očekuje se da će u narednom periodu Omisirge imati veliki udeo u odrađenim transplantacijama matičnih ćelija čime će se značajno povećati primena matičnih ćelija iz pupčanika.
Omisirge su pojedini poznavaoci ove oblasti medicine nazvali „Grifon” – mitskim bićem, zveri koja ima prednje noge orla, a zadnje lava jer kombinuje sve najbolje karakteristike matičnih ćelija svih izvora.
Naime, dobijen je proizvod koji ima najbolje karakteristike ćelija koštane srži, periferne krvi i krvi pupčanika.
Vreme usađivanja kraće što uliva nadu pacijenatima
Omisirge ima osobine matičnih ćelija iz koštane srži kada je u pitanju usađivanje matičnih ćelija, čak po studijama ovo vreme je kod Omisirge-a značajno kraće (srednje vreme usađivanja neutrofila je desetak dana) od ćelija iz koštane srži (15-17 dana). Srednje vreme usađivanja matičnih ćelija iz pupčanika je 20-24 dana.
Smanjenjem broja dana potrebnih za usađivanje transplantata u značajnoj meri se snižava rizik od infekcija kod pacijenata koji su imunokompromitovani.
Omisirge je zadržao superiorne osobine krvi pupčanika kada je u pitanju najveći stepen preživljavanja pacijenata i najmanji broj bolesti graft protiv domaćina u odnosu na koštanu srž i perifernu krv.
Dostupan u deset bolnica u SAD-u
U SAD-u će Omisirge biti dostupan u desetak najvećih bolnica koje rade transplantacije matičnih ćelija, a i najveće osiguravajuće kuće će pokrivati troškove Omisirge-a jer je ovo jednokratna terapija koja najčešće vodi potpunom izlečenju čime se značajno smanjuju troškovi dosadašnjih transplantacija.
Put do registracije Omisirge-a je bio dug, nimalo lak i jako skup. Gamida je sprovela više od deset kliničkih studija od 2007. godine, a FDA je ekstremno oprezna u pogledu odobravanja bioloških proizvoda koji se prave od živih ćelija.
Omisirge se ovim pridružuje ćelijskim produktima dobijenim od matičnih ćelija poput CAR-T proizvoda i nekoliko genskih terapija za teške genetske bolesti koje su već zvanično odobrene od strane FDA i evropskih agencija za lekove.
Za industriju krvi pupčanika ovo je istorijski trenutak.
.jpg)
.jpg) Foto: Freepik
Foto: Freepik















































































































































Komentari (0)